镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下: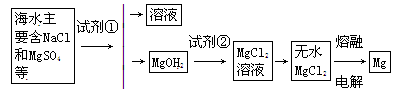
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用 。试剂②可以选用 。
(2)验证MgCl2已完全转化为Mg(OH)2的方法是 。
(3)由MgCl2溶液得到无水MgCl2的方法是 。
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用 。试剂②可以选用 。
(2)验证MgCl2已完全转化为Mg(OH)2的方法是 。
(3)由MgCl2溶液得到无水MgCl2的方法是 。