某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题: 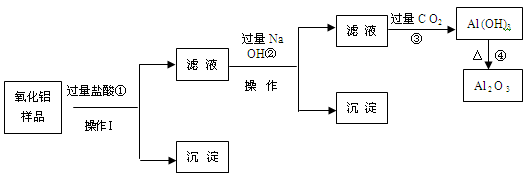
(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:
、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题: 
(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:
、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。