可逆反应A(g)+B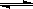 C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
| A.若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体 |
| B.若升高温度,发现C的物质的量减少,则说明正反应为放热反应 |
| C.若压缩容器,平衡不移动,则说明B和D一定都是气体 |
| D.保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少 |
可逆反应A(g)+B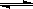 C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
| A.若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体 |
| B.若升高温度,发现C的物质的量减少,则说明正反应为放热反应 |
| C.若压缩容器,平衡不移动,则说明B和D一定都是气体 |
| D.保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少 |