有A、B、C、D四种短周期元素在周期表中相对位置如右图:
(1)A与D形成的液态化合物是常见的重要有机溶剂,则A、B、C、D四种元素最高价氧化物对应的水化物酸性由强到弱的顺序是:_______>_________>___________>______(用化学式表示),B、C、D三种元素的第一电离能由大到小的顺序是:______________(用元素符号表示)(2)X、Y为C、D两种元素形成的单质。标准状况下,X的密度为3.17 g/L。Z是一种化合物,焰色反应呈紫色(透过蓝色钴玻璃),室温下0.1 mol/L Z水溶液pH=13。X、Y、Z有如图转化关系:
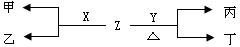
①写出X与Z反应的离子方程式:_____________________________
②已知丙能与稀硫酸反应生成使品红褪色的气体。丁的化学式_______,丁的水溶液pH>7的原因:___________________________________(用离子方程式表示)
③将20 mL 0.5 mol/L丙溶液逐滴加入20 mL 0.2 mol/L KMnO4溶液(硫酸酸化)中,恰好褪色。写出反应的离子方程式_________。