(1)已知:Fe(s)+1/2O2(g)═2FeO(s) △H1=-272.0kJ•mol-1 ①;
2Al(s)+3/2O2(g)═Al2O3(s)△H2=-1675.7kJ•mol-1 ②
Al和FeO发生铝热反应的热化学方程式是 。
(2)某可逆反应在不同条件下的反应历程分别为A、B,如图所示。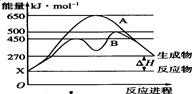
①据图判断该反应达到平衡后,其他条件不变,升高温度,反应物的转化率 (填“增大”“减小”或“不变”)。
②其中B历程表明此反应采用的条件为 (选填序号)。
A.升高温度
B.增大反应物的浓度
C.降低温度
D.使用催化剂
(3)1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)。该反应的平衡常数表达式为 ;已知K1000℃< K1200℃,若降低体系温度,混合气体的平均相对分子质量将会 (填“增大”“减小”或“不变”)。
Na2S(s)+4H2O(g)。该反应的平衡常数表达式为 ;已知K1000℃< K1200℃,若降低体系温度,混合气体的平均相对分子质量将会 (填“增大”“减小”或“不变”)。
(4)常温下,如果取0.1 mol/LHA溶液与0.1 mol/lNaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。
①混合液中由水电离出的OH一浓度与0.1 mol/lNaOH溶液中由水电离出的OH一浓度之比为 。
②已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,
试推断(NH4)2 CO3溶液的pH (填“<”“>”或“=”)7;
相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排列顺序为 (填序号)。
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl
 CH3OH(g)
CH3OH(g)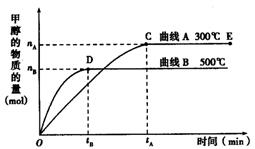
 CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:

 粤公网安备 44130202000953号
粤公网安备 44130202000953号