某同学为了验证Fe3+是否能氧化H2SO3生成了SO42–,他用50mL0.1mol/LFeCl3溶液吸收制取SO2气体的尾气,再进行以下实验:
(1)检验吸收液中的SO42–: ,
则证明Fe3+能把H2SO3氧化为SO42–。
(2)请配平并完成上述反应中的化学方程式:
2FeCl3+SO2+ ==2FeCl2+H2SO4+2HCl,反应中的氧化产物是 (写化学式)。
(3)吸收液中除了含有H+、Cl–、SO42–以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。 假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在 ;
假设3:溶液中存在Fe2+ 而不存在H2SO3(二者恰好完全反应)。
②设计方案、进行实验,验证假设。请在表中写出实验步骤以及预期现象和结论(可以不填满)。限选实验试剂和仪器:试管、滴管、0.1moL L-1KMnO4、0.1moL
L-1KMnO4、0.1moL L-1KSCN溶液、品红溶液。
L-1KSCN溶液、品红溶液。
| 实验步骤 |
预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,再用滴管取 |
若出现血红色,则假设1成立; (2)若未出现血红色,则假设2或假设3成立。 |
| 步骤2: |
|


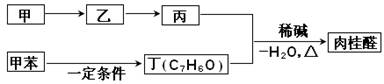

 2Cu+SO2
2Cu+SO2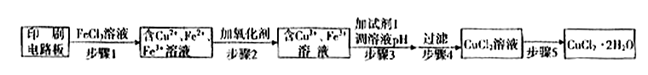 ①证明步骤I所加FeCl3溶液过量的方法是。
①证明步骤I所加FeCl3溶液过量的方法是。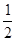 O2(g)==H2O(l)△H3=-286kJ/mol
O2(g)==H2O(l)△H3=-286kJ/mol
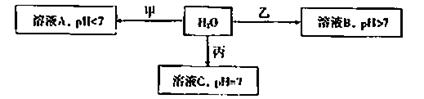
 物或生成物已略去):
物或生成物已略去):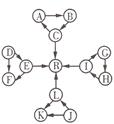
 回答下列问题:
回答下列问题: 2)写出下列反应的离子方程式:
2)写出下列反应的离子方程式: 粤公网安备 44130202000953号
粤公网安备 44130202000953号