(1)请根据官能团的不同对下列有机物进行分类:
①(CH3)3CCH2OH ②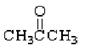 ③
③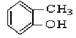
④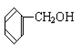 ⑤
⑤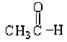 ⑥
⑥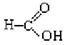
上述物质中,属于芳香醇的是 ,属于酚类的是 属于羧酸类的是 ,属于醛类的是 (填序号)
(2)下列属于同系物的是 ,属于同分异构体的是 (填入编号)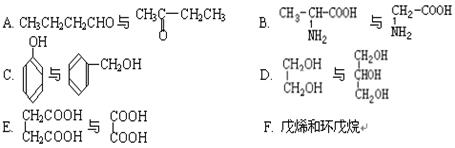
(1)请根据官能团的不同对下列有机物进行分类:
①(CH3)3CCH2OH ②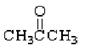 ③
③
④ ⑤
⑤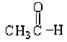 ⑥
⑥
上述物质中,属于芳香醇的是 ,属于酚类的是 属于羧酸类的是 ,属于醛类的是 (填序号)
(2)下列属于同系物的是 ,属于同分异构体的是 (填入编号)