(10分)一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。
(1)加入铝粉产生H2,说明铝具有______(填“氧化性”或“还原性”)。
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在。
设计实验证实如下:
| 装 置 |
现 象 |
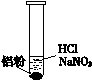 |
ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,液面上方呈浅棕色 ⅲ. 试管变热,溶液沸腾 |
| 实验 |
内容 |
现象 |
| 实验1 |
将湿润KI—淀粉试纸置于空气中 |
未变蓝 |
| 实验2 |
用湿润KI—淀粉试纸检验浅棕色气体 |
试纸变蓝 |
①盐酸溶解Al2O3薄膜的离子方程式是____ __。
②根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
a.浅棕色气体是______。
b.实验1的目的是_ 。
c.实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整: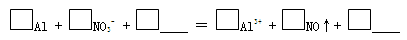
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。
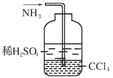
重新设计实验证实如下:
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
① 刺激性气味的气体是________________。 ② 产生该气体的离子方程式是__ 。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是__ ____。
(5)实验结果证实:NO3‑在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。习题中的无色溶液一定能大量存在的是Na+和OH-。





 粤公网安备 44130202000953号
粤公网安备 44130202000953号