氮是一种重要的非金属元素,可以形成多种不同类型的化合物,请根据要求回答下列问题:
(1)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,
①写出该反应的化学方程式 .
若反应中生成0.2 mol HNO3,转移的电子数目为________个.
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F 据题意推测 NF3,F2,NO三种气体中,氧化性由弱到强的顺序为
(2)已知工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3~0.5g.已知NaNO2能发生如下反应(方程式已配平):
2NO2—+xI—+yH+=2NO↑+I2+zH2O,
①根据上述反应,鉴别NaNO2和NaCl可选用的物质有:
A.碘化钾淀粉试纸 B.淀粉 C.食醋 D.白酒
你认为必须选用的物质有_________(填序号)。
②某工厂废切削液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是________________。
A.NaCl B.KMnO4 C.浓硫酸 D.NH4Cl
(3)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平,不考虑2NO2 N2O4)。0.004molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为____________;所得溶液(假设溶质不扩散)的物质的量浓度是___________ 。
N2O4)。0.004molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为____________;所得溶液(假设溶质不扩散)的物质的量浓度是___________ 。


 (V)的关系如图所示
(V)的关系如图所示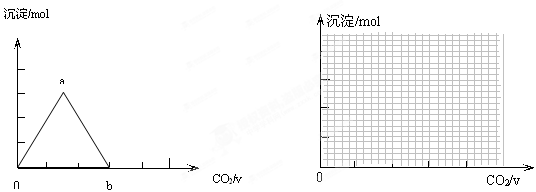
 式;
式;
 粤公网安备 44130202000953号
粤公网安备 44130202000953号