三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
I.铁含量的测定
步骤一:称量5.00 g三草酸合铁酸钾晶体,配制成250 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010 mol·L—1KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02 mL,滴定中MnO4—被还原成Mn2+。
重复步骤二、步骤三操作,滴定消耗0.010 mol/L KMnO4溶液19.98 mL
请回答下列问题:
(1)步骤一中配制三草酸合铁酸钾溶液使用到的玻璃仪器包括:烧杯、玻璃棒、
(2)步骤二中加入锌粉至黄色刚好消失,目的是___________________________。
(3)写出步骤三中发生反应的离子方程式 _________________ 。
(4)根据实验数据,测得该晶体中铁元素的质量分数为__________________________________。
(5)若步骤二中加入的KMnO4的溶液的量不足,则测得的铁含量 (选填填“偏低”“偏高”或“不变”)
II.结晶水的测定
(6)采用热重分析仪测定三革酸合铁酸钾晶体K3[Fe(C2O4)3]·xH2O在100℃时的失重率为a%,则晶体化学式中结晶水的个数x的计算式为_________________(已知:三草酸合铁酸钾的摩尔质量M(K3[Fe(C2O4)3]) =510g/mol)

 (图3)
(图3)
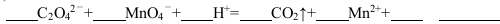
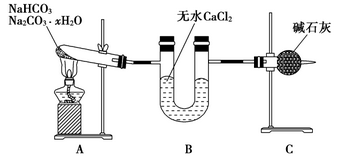
 Na2CO3 + CO2↑+ H2O②含结晶水的物质加热易失去结晶水
Na2CO3 + CO2↑+ H2O②含结晶水的物质加热易失去结晶水 CH3Cl+H2O.具体步骤如下:
CH3Cl+H2O.具体步骤如下: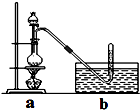

 粤公网安备 44130202000953号
粤公网安备 44130202000953号