在25℃时,有pH=a(a≤6)的盐酸VaL和pH=b(b≥8)的NaOH溶液VbL。二者混合恰好完全中和。问:
(1)若a+b=14时,则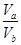 =________(填数值);
=________(填数值);
(2)若a+b=13时,则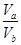 =________(填数值);
=________(填数值);
(3)若a+b>14时,则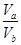 =________(填表达式),且Va Vb(填“>”“<”或“=”)
=________(填表达式),且Va Vb(填“>”“<”或“=”)
在25℃时,有pH=a(a≤6)的盐酸VaL和pH=b(b≥8)的NaOH溶液VbL。二者混合恰好完全中和。问:
(1)若a+b=14时,则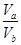 =________(填数值);
=________(填数值);
(2)若a+b=13时,则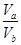 =________(填数值);
=________(填数值);
(3)若a+b>14时,则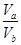 =________(填表达式),且Va Vb(填“>”“<”或“=”)
=________(填表达式),且Va Vb(填“>”“<”或“=”)