周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子排布式为 。
(2)a和上述元素中的一种元素形成的共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;上述元素形成的分子中既含有极性共价键、又含有非极性共价键的化合物是 (填化学式)。
(3)这些元素形成的含氧酸中,酸根中的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥形结构的酸是 。(均填化学式)
(4)e和c形成的一种离子化合物的晶体的晶胞结构(图1),则e的化合价为 。
(5)这5种元素形成的一种阴阳离子数比为1:1的离子化合物中,阴离子呈四面体结构;阳离子呈狭长的八面体结构(图2)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 。
(6)根据e晶胞结构(图3),e晶胞中每个e原子周围距离最近的e原子数目为 。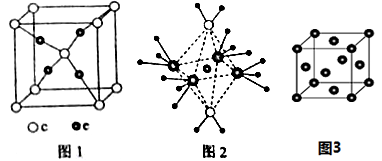
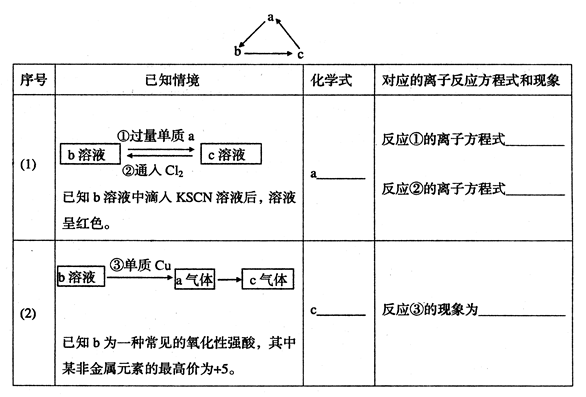
 程中能量变化示意图,写出NO2和CO反应的热化学方程式。
程中能量变化示意图,写出NO2和CO反应的热化学方程式。
 O2(g)=CO2(g)的△H=kJ·mol-1
O2(g)=CO2(g)的△H=kJ·mol-1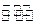 2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 m01.则前5分钟的平均反应速率v(N2)为
2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 m01.则前5分钟的平均反应速率v(N2)为 ,平衡时H2的转化率为%,该反应的平衡常数K=(mol·L-1)-2.
,平衡时H2的转化率为%,该反应的平衡常数K=(mol·L-1)-2.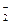 + xI-+ yH+= 2NO↑+ I2 + zH2O,请回答下列问题:
+ xI-+ yH+= 2NO↑+ I2 + zH2O,请回答下列问题: 含有2%—5%的NaNO2,直接排放会造成水污染,但加入下列
含有2%—5%的NaNO2,直接排放会造成水污染,但加入下列 。
。 。(填化学式)
。(填化学式) 粤公网安备 44130202000953号
粤公网安备 44130202000953号