(共14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1)从①组分析,HA是 酸(填强或弱)。所得混合溶液由水电离出c(OH-) = mol·L-1。
(2)②组表明,c 0.2(选填“>、=或 <”)。
该混合液中离子浓度c(A-)与c(Na+)的大小关系是 。(选填“>、=或 <”)
(3)从③组分析,说明此时HA电离程度 NaA水解程度(选填“>、=或 <”)。
该混合溶液中各离子浓度由大到小的顺序是 。
(4)由上述所涉及的溶质组成以下四组等体积溶液:
甲:0.1mol/LNaA; 乙:0.1mol/LNaA和0.1mol/LHA;
丙:0.1mol/LHA; 丁:0.1mol/LNaA和0.1mol/LNaOH;
则A-离子浓度由大到小的顺序为 > > > 。(填写序号)
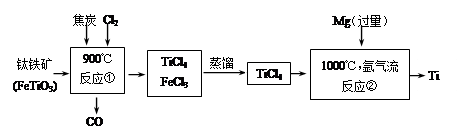
 H2↑+Cl2↑ ______________________________
H2↑+Cl2↑ ______________________________ _______+________
_______+________
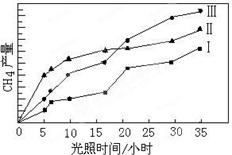
 CO(g)+3H2(g),该反应的ΔH="+206" kJ•mol-1将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率(计算结果保留两位有效数字)
CO(g)+3H2(g),该反应的ΔH="+206" kJ•mol-1将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率(计算结果保留两位有效数字) 粤公网安备 44130202000953号
粤公网安备 44130202000953号