用二氧化氯(ClO2)新型净水剂替代传统的净水剂Cl2,对淡水进行消毒是城市饮用水处理的新技术。
(1)已知ClO2在水处理过程中被还原为Cl-。若以单位质量的氧化剂所得到的电子数来表示消毒效率,则ClO2、Cl2两种消毒剂的消毒效率由小到大的顺序是。(填化学式)
(2)ClO2的制备方法:
①工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目。
②纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物Y与NaClO3反应生成ClO2。完成反应的化学方程式:
□(Y)+24NaClO3+12H2SO4 =□ClO2↑+□CO2↑+18H2O+□________,假设该反应在标准状况下生成1.12 L气体,则转移的电子数为。
③实验室通常以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
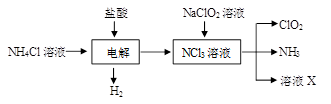
推测溶液X为。
(3)ClO2是一种黄绿色有刺激性气味的气体,实验室通常用NaOH溶液来吸收ClO2,以减少环境污染。若实验时需要450mL 4mol/L的NaOH溶液,则配制时,需要用托盘天平称取NaOH的质量为___g,所使用的仪器除托盘天平、胶头滴管、玻璃棒外,还必须有。配制该溶液时,下列操作会使溶液浓度偏高的是。(填字母)
| A.称量固体时动作缓慢 |
| B.容量瓶未干燥立即用来配制溶液 |
| C.NaOH固体溶解后立刻转移 |
| D.在容量瓶中定容时俯视容量瓶刻度线 |
E.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线