由金红石(TiO2)制取单质Ti,涉及到的步骤为: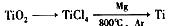
已知:① C(s) + O2(g) ="=" CO2(g); △H = -393.5 kJ•mol-1
② 2CO(g) + O2(g) ="=" 2CO2(g); △H = -566 kJ•mol-1
③ TiO2(s) + 2Cl2(g) ="=" TiCl4(s) + O2(g); △H =" +141" kJ•mol-1
(1)则TiO2(s) + 2Cl2(g) + 2C(s)="=" TiCl4(s) + 2CO(g) 的△H = _________________。
(2)反应TiCl4 + 2Mg ="=" 2MgCl2 + Ti 在Ar气氛中进行的理由是_____________。