在实验室里配制100
10%的
溶液,操作如下图,请回答下列问题:
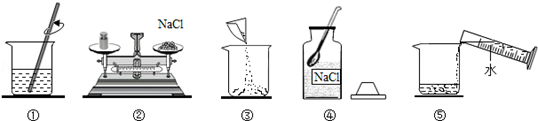
(1)认真观察,指出图中错误的操作步骤(填序号);
(2)配制该溶液需要
固体
,需要水
(ρ水=1g/mL),需要用
的量筒(填"50
"、"100
"或"200
")量取.
在实验室里配制100
10%的
溶液,操作如下图,请回答下列问题:

(1)认真观察,指出图中错误的操作步骤(填序号);
(2)配制该溶液需要
固体
,需要水
(ρ水=1g/mL),需要用
的量筒(填"50
"、"100
"或"200
")量取.