(3分)已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。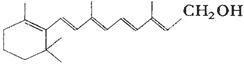
请回答下列问题:
(1)维生素A1是一类重要的维生素,写出其含氧官能团的名称 。
(2)维生素A1的结构简式如上图,若1mol维生素A1分子最多可跟__ molH2发生加成反应
四、简答题(本题有2小题,共11分)
(3分)已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。
请回答下列问题:
(1)维生素A1是一类重要的维生素,写出其含氧官能团的名称 。
(2)维生素A1的结构简式如上图,若1mol维生素A1分子最多可跟__ molH2发生加成反应
四、简答题(本题有2小题,共11分)