合成氨反应是“将空气变成面包”的反应,如果没有合成氨反应,地球将无法养活现在这么多的人。已知合成氨的反应为N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
Ⅰ.在体积为5 L的恒温、恒容密闭容器甲中,起始时投入2 mol N2、3 mol H2,经过10 s达到平衡,测得平衡时NH3的物质的量为0.8 mol。
Ⅱ.在容器乙中,起始时投入3 mol N2、b mol H2,维持恒温、恒压达到平衡,测得平衡时NH3的物质的量为1.2 mol。此时与容器甲中平衡状态温度相同,相同组分的体积分数都相同。
(1)容器甲10 s内用H2表示的平均反应速率v(H2)=_________,达平衡时 N2的转化率=__________。
(2)甲容器中反应的逆反应速率随时间变化的关系如图。t2时改变了某一种条件,改变的条件可能是________、______(填写两项)。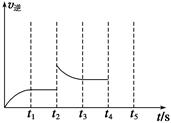
(3)下列哪些情况表明容器乙已达平衡状态__________(填字母)。
A容器乙中的气体密度不再变化
B反应的平衡常数不再变化
C氨气的生成速率等于氮气的消耗速率的2倍
D断裂1 mol N≡N键同时断裂6 mol N—H键
E.容器乙中气体的平均相对分子质量不随时间而变化
(4)b=__________。

 2NH3(g) ΔH=-92.2 kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6 L NH3时,放出的热量为________。
2NH3(g) ΔH=-92.2 kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6 L NH3时,放出的热量为________。

 不变
不变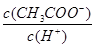 减小
减小 H++HA-,HA-
H++HA-,HA- H++A2-。回答以下问题:某温度下,向0.1 mol·L-1的NaHA酸性溶液中滴入0.1 mol·L-1 KOH溶液至中性,此时溶液中以下所示关系一定正确的是________。
H++A2-。回答以下问题:某温度下,向0.1 mol·L-1的NaHA酸性溶液中滴入0.1 mol·L-1 KOH溶液至中性,此时溶液中以下所示关系一定正确的是________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号