(1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g) 2NH3(g) △H<0达到平衡的标志是__________________________(填编号)
2NH3(g) △H<0达到平衡的标志是__________________________(填编号)
①反应速率v(N2):v(H2):v(NH3) =" 1" : 3 : 2 ②各组分的物质的量浓度不再改变
③体系的压强不再发生变化 ④混合气体的密度不变
⑤单位时间内生成n mol N2的同时,生成3n mol H2
⑥2V(N2正)= V(NH3逆)
⑦单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
⑧混合气体的平均相对分子质量不再改变
(2)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下图所示。已知在反应过程中混合气体的平均分子量没有变化。请回答: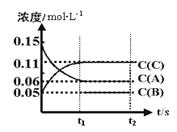
①密闭容器的体积是 L。
②若t1=15s时,则t0-t1阶段以C物质浓度变化表示的反应速率为v(C)= 。
③写出反应的化学方程式: 。
④B的起始物质的量是 。
(3)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: 。若1g水蒸气转化为液态水放热2.44kJ,则反应2H2(g)+O2(g) =2H2O(l) △H= kJ∙mol-1。
相关知识点
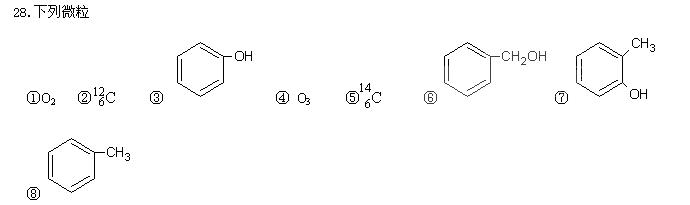 (1)属于同位素的是(填编号,下同)
(1)属于同位素的是(填编号,下同) 、AlCl3、CuCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体
、AlCl3、CuCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体 体积数据已换算成标准状况下的体积):
体积数据已换算成标准状况下的体积):
 算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程)。
算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程)。 的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。
的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。
 为
为 固体时,X与A反应的化学方程式为
固体时,X与A反应的化学方程式为 冷水反应,在标准状况下生成11.2LH2
冷水反应,在标准状况下生成11.2LH2 __;(用离子符
__;(用离子符 号和“>”、“=”或“<”表示)
号和“>”、“=”或“<”表示) 写化学式,下同),既含离子键又含共价键的是______________。
写化学式,下同),既含离子键又含共价键的是______________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号