有一种工业废水,其中含有大量的硫酸亚铁、少量硫酸铜和污泥。某同学设计了一个既经济又合理的实验方案,制备硫酸亚铁晶体(
)并回收铜。方案流程如下:
【查阅资料】
受热易分解。
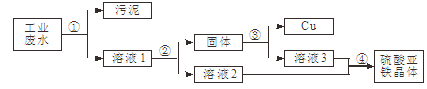
回答下列问题:
(1)步骤①中用到的玻璃仪器有烧杯、漏斗和
(2)步骤②中需加入的物质是
(3)步骤③中发生反应的化学方程式是
(4)步骤④的操作是蒸发浓缩、
有一种工业废水,其中含有大量的硫酸亚铁、少量硫酸铜和污泥。某同学设计了一个既经济又合理的实验方案,制备硫酸亚铁晶体(
)并回收铜。方案流程如下:
【查阅资料】
受热易分解。

回答下列问题:
(1)步骤①中用到的玻璃仪器有烧杯、漏斗和
(2)步骤②中需加入的物质是
(3)步骤③中发生反应的化学方程式是
(4)步骤④的操作是蒸发浓缩、