如图为以惰性电极进行电解的串联电解装置图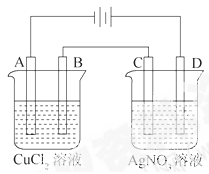
(1)写出A、B、C、D各电极上的电极方程式。
A ;
B ;
C ’
D 。
(2)在A、B、C、D各电极上析出生成物的物质的量比为 。
如图为以惰性电极进行电解的串联电解装置图
(1)写出A、B、C、D各电极上的电极方程式。
A ;
B ;
C ’
D 。
(2)在A、B、C、D各电极上析出生成物的物质的量比为 。