A、B、C、D、E、F是初中化学常见的六种物质,化学兴趣小组同学设计了下图所示的接龙游戏,箭头表示一种物质可以转化成另一种物质。若常温下A是一种无色液体,B、C为无色无味气体;A转化成E为放热反应,且E、F物质类别相同,D与E反应可生成F。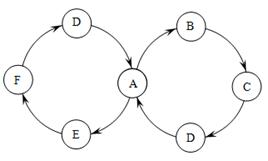
⑴写出下列物质的化学式:
A ,C 。
⑵写出下列化学方程式:
①A转化成B的反应 ;
②D与E生成F的反应 。
A、B、C、D、E、F是初中化学常见的六种物质,化学兴趣小组同学设计了下图所示的接龙游戏,箭头表示一种物质可以转化成另一种物质。若常温下A是一种无色液体,B、C为无色无味气体;A转化成E为放热反应,且E、F物质类别相同,D与E反应可生成F。
⑴写出下列物质的化学式:
A ,C 。
⑵写出下列化学方程式:
①A转化成B的反应 ;
②D与E生成F的反应 。