用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
(1) SiCl4的平均反应速率为___
(2)平衡后,若改变温度,混合气体的平均相对分子质量与温度的关系如图所示,下列说法正确的是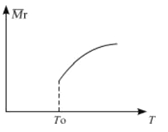
| A.该反应在任何温度下可自发进行 |
| B.若混合气体的总质量不变,表明上述反应己达到平衡状态 |
| C.其他条件不变,增大Si3N4的物质的量,平衡向左移动 |
| D.按3:2:6的物质的量比增加反应物,SiC14(g)的转化率降低 |
(3)下表为不同温度下该反应的平衡常数,其他条件相同时,在___(填"T1”、“T2”.,“T3”)温度下反应达到平衡所需时间最长:
假设温度为T1时向该反应容器中同时加入。(SiC14) =0.3 mol/L,c(H2) =0.3 mol/L,,c(N2) =
x mol/L, c (HCl) =0.3 mol/L和足量Si3N4 (s),若要使平衡建立的过程中HCl浓度减小,x的取值
范围为___
(4)该反应的原子利用率为____
(5)工业上制备SiCl4的反应过程如下: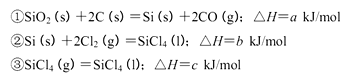
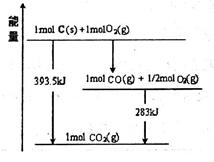
写出二氧化硅、焦炭与Cl 2在高温下反应生成气态SiC14和一氧化碳的热化学方程式_____

 2C(g) ΔH < 0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是 (填序号字母)
2C(g) ΔH < 0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是 (填序号字母)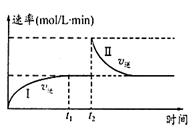
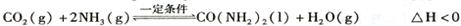

 N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
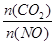 增大的措施有__________(任写一条)。
增大的措施有__________(任写一条)。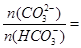 ________。
________。 NaBr+NaBrO3+NaHCO3,吸收1 mol Br2时转移的电子为__ mol。
NaBr+NaBrO3+NaHCO3,吸收1 mol Br2时转移的电子为__ mol。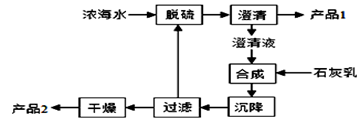

 CO2(g)+H2(g) ΔH=-41 kJ/mol
CO2(g)+H2(g) ΔH=-41 kJ/mol
 粤公网安备 44130202000953号
粤公网安备 44130202000953号