某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或“不是”);
(3)已知A、B、C有如下转化关系: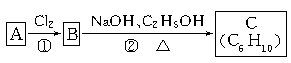
则反应②的化学方程式为 ;C的化学名称是 。
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或“不是”);
(3)已知A、B、C有如下转化关系: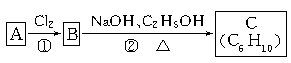
则反应②的化学方程式为 ;C的化学名称是 。