根据下列条件计算有关反应的焓变:
(1)已知:
Ti(s)+2Cl2(g)===TiCl4(l) ΔH=-804.2 kJ·mol-1
2Na(s)+Cl2(g)==="2NaCl(s)" ΔH=-882.0 kJ·mol-1
Na(s)===Na(l) ΔH=+2.6 kJ·mol-1
则反应TiCl4(l)+4Na(l)===Ti(s)+4NaCl(s)的ΔH= kJ·mol-1。
(2)已知下列反应数值:
| 序号 |
化学反应 |
反应热 |
| ① |
Fe2O3(s)+3CO(g)=== 2Fe(s)+3CO2(g) |
ΔH1=-26.7 kJ·mol-1 |
| ② |
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) |
ΔH2=-50.8 kJ·mol-1 |
| ③ |
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) |
ΔH3=-36.5 kJ·mol-1 |
| ④ |
FeO(s)+CO(g)===Fe(s)+CO2(g) |
ΔH4 |
则反应④的ΔH4= kJ·mol-1。
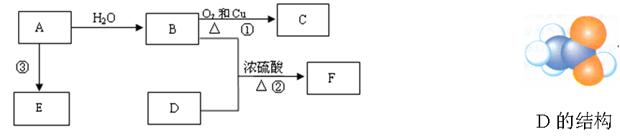
 ;
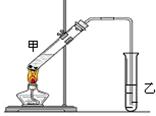
;
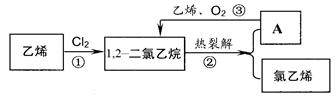
 的中间体——草酸二乙酯(C2H5OOCCOOC2H5)(用反应流程图表示,并注明反应条件)。
的中间体——草酸二乙酯(C2H5OOCCOOC2H5)(用反应流程图表示,并注明反应条件)。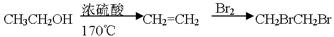
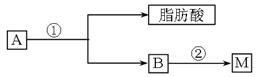
 C2H5O-NO2+H2O
C2H5O-NO2+H2O 分子式为________________。
分子式为________________。 能的结构简式:________________________________________________。
能的结构简式:________________________________________________。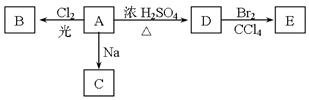
 内A的各种变化,且F烃基上的一氯取代物有三种。F的结构简式是___________________________________________。
内A的各种变化,且F烃基上的一氯取代物有三种。F的结构简式是___________________________________________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号