随着电子工业的发展,电子垃圾的数量逐渐增多,对环境构成了极大的污染。某化学兴趣探究小组将一批废弃的线路板简单处理后,得到红色金属M和金属E并进行如下框图所示转化,获得高效净水剂K2EO4。(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):
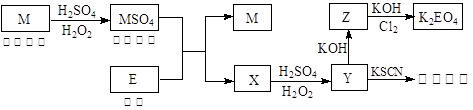
(1)写出Z与Cl2、KOH反应生成K2EO4的离子方程式: 。
(2)检验X中阳离子的方法和现象是 。
(3)如果各步转化无损失,M转化为MSO4消耗的H2O2与X转化为Y消耗的H2O2的用量之比为:
。
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、蒸发皿、铁架台外,还需要用到的玻璃仪器有 、 、 (填写仪器名称)。
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图,A中试剂是盐酸。
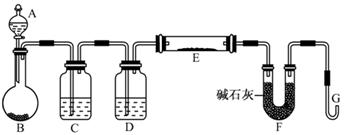
①如果去掉装置C,则测定的M的相对原子质量 (填写偏高、偏低、正常),装置D的作用 ;
②连接好装置并检验装置的气密性,检验气密性的方法是:
。
然后应首先“加热反应管E”还是“从A瓶中逐滴加入液体” ? 在这两步之间还应进行的操作是 。
 aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。
aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。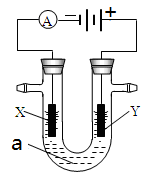
 2K2CO3+6H2O
2K2CO3+6H2O
 粤公网安备 44130202000953号
粤公网安备 44130202000953号