I. 铜铁及其化合物在日常生活中应用广泛,某研究性学习小组用粗铜(含杂质Fe)与过量氯气反应得固体A,用稀盐酸溶解A,然后加试剂调节溶液的pH后得溶液B,溶液B经系列操作可得氯化铜晶体,请回答:
(1)溶液B经过 、 、 可得到氯化铜晶体;
(2)检验溶液B中是否存在Fe3+的方法是 ;
(3)下列物质适合于调节溶液的pH得溶液B的是
A.NaOH溶液 B.CuCO3 C.氨水 D CuO
(4)已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是 ;
II. (1)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷
酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料。
①若氨水与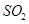 恰好完全反应生成正盐,则此时溶液呈________性(填“酸”或“碱”)。
恰好完全反应生成正盐,则此时溶液呈________性(填“酸”或“碱”)。
常温下弱电解质的电离平衡常数如下:氨水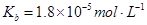
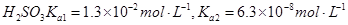
②向②中溶液中通入________气体可使溶液呈中性。(填“SO2”或NH3”)此时溶液中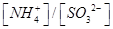 ________2(填“>”“<”或“=”)
________2(填“>”“<”或“=”)
(2)向0.2mol•L‾1 NaOH 溶液通入过量CO2,充分反应后所得溶液中离子浓度大小顺序为
___________________________________ 。
 金属铝的生产是以Al2O3为原料,在熔融状态下进行电解:
金属铝的生产是以Al2O3为原料,在熔融状态下进行电解: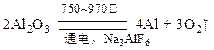
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: t
t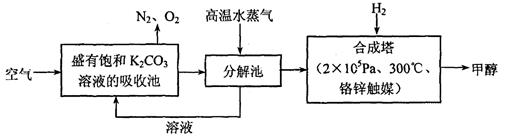
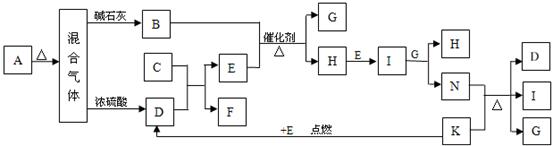
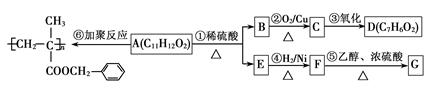
 _______。
_______。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号