工业上常用铬铁矿(有效成份为FeO·Cr2O3,主要杂质为SiO2、Al2O3)为原料生产重铬酸钾(K2Cr2O7),实验室模拟工业法用铬铁矿制重铬酸钾的主要工艺流程如下图,涉及的主要反应是:6FeO·Cr2O3+24NaOH+7KClO3=12Na2CrO4+3Fe2O3+7KCl+12H2O,试回答下列问题:
(1)⑤中溶液金属阳离子的检验方法是 。
(2)步骤③被沉淀的离子为(填离子符号) 。
(3)在反应器①中,二氧化硅与纯碱反应的化学方程式为: 。
(4)烟道气中的CO2可与H2合成甲醇。CH3OH、H2的燃烧热分别为:ΔH=-725.5 kJ/mol、ΔH=-285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
(5)2011年云南曲靖的铬污染事件,说明含铬废渣(废水)的随意排放对人类生存环境有极大的危害。电解法是处理铬污染的一种方法,金属铁作阳极、石墨作阴极电解含Cr2O72-的酸性废水,一段时间后产生Fe(OH)3和Cr(OH)3沉淀。
①写出电解法处理废水的总反应的离子方程式 。
②已知Cr(OH)3的Ksp=6.3×10–31,若地表水铬含量最高限值是0.1 mg/L,要使溶液中c(Cr3+)降到符合地表水限值,须调节溶液的c(OH-)≥ mol/L(只写计算表达式)。
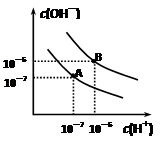
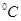 时水的电离平衡曲线应为(填“A”或“B”)。
时水的电离平衡曲线应为(填“A”或“B”)。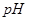 =8的NaOH溶液与
=8的NaOH溶液与 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的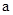 的某强酸溶液与1体积
的某强酸溶液与1体积 xC(g) △H>0,达到化学平衡后,C的体积分数为a。
xC(g) △H>0,达到化学平衡后,C的体积分数为a。 mC(g);变化如下图所示。已知坐标表示在不同温度和压强下生成物C在混合物中的质量分数,P为反应在T2温度时达到平衡后向容器加压的变化情况,问:
mC(g);变化如下图所示。已知坐标表示在不同温度和压强下生成物C在混合物中的质量分数,P为反应在T2温度时达到平衡后向容器加压的变化情况,问: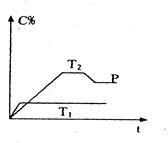

 粤公网安备 44130202000953号
粤公网安备 44130202000953号