如图所示,分馏装置中,如果有错误请指出并加以改正: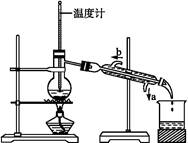
(1) _____________________________,
(2) _____________________________,
(3) _____________________________。
如图所示,分馏装置中,如果有错误请指出并加以改正:
(1) _____________________________,
(2) _____________________________,
(3) _____________________________。