某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题: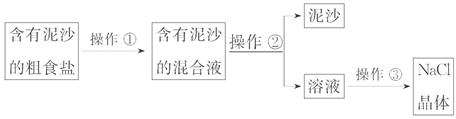
(1)操作①、②、③依次为下图中的(填字母) 。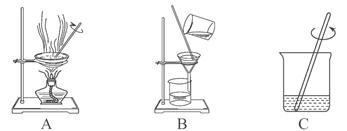
(2)若NaCl的产率偏低( ),则可能的原因是(填字母) 。
),则可能的原因是(填字母) 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5% NaCl溶液50.0 g,需称取NaCl g,配制时需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。
某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
(1)操作①、②、③依次为下图中的(填字母) 。
(2)若NaCl的产率偏低( ),则可能的原因是(填字母) 。
),则可能的原因是(填字母) 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5% NaCl溶液50.0 g,需称取NaCl g,配制时需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。