a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族。a的原子结构示意图为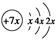 ,b与d形成的化合物的电子式为
,b与d形成的化合物的电子式为 ,则下列叙述中正确的是
,则下列叙述中正确的是
( )。
| A.原子序数:a>b>c | B.d单质最活泼 |
| C.原子半径:a>c>d | D.最高价氧化物对应的水化物的酸性:d>a>c |
a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族。a的原子结构示意图为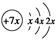 ,b与d形成的化合物的电子式为
,b与d形成的化合物的电子式为 ,则下列叙述中正确的是
,则下列叙述中正确的是
( )。
| A.原子序数:a>b>c | B.d单质最活泼 |
| C.原子半径:a>c>d | D.最高价氧化物对应的水化物的酸性:d>a>c |