氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式为________。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为________L。
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮做氧化剂,反应产物是氮气和水。由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,则推进剂中联氨的质量________。
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O 6NO2+ 8NH3=7N2+12H2O。NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。则①该混合气体中NO与NO2的体积比为________,②吸收后氨水的物质的量浓度________(答案保留1位小数)。

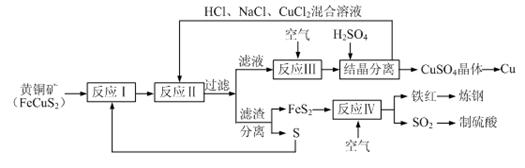
 3++
3++  Fe3++ H2O(未配平)
Fe3++ H2O(未配平)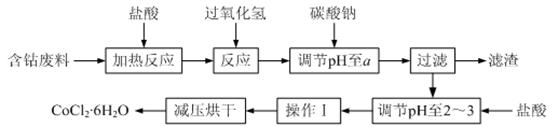
 10
10 ~120℃时,失去结晶水变成有毒的无水氯化钴。
~120℃时,失去结晶水变成有毒的无水氯化钴。 干的原因是 ▲。
干的原因是 ▲。
 数(%)
数(%) 6
6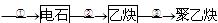
 。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________________。
。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________________。
 ④ 取代反应
④ 取代反应 ________________。
________________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号