由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图的转化关系,已知C为密度最小的气体,甲为非电解质。
根据以上转化关系回答下列问题: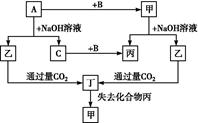
(1)写出下列物质的化学式:A ,B ,丁 。
(2)元素A在周期表中的位置是 ,写出甲的一种用途 。
(3)写出下列变化的方程式:
①A与NaOH溶液反应的化学方程式 。
②乙与过量CO2反应的离子方程式 。
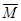 (混)
(混)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号