运用化学反应原理知识在工业生产中有重要意义。
(1) 工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___________ _____。
(2)工业生产中用CO可以合成甲醇CO(g)+2H2(g)  CH3OH(g),ΔH=-90.1 kJ·mol-1 在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
CH3OH(g),ΔH=-90.1 kJ·mol-1 在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=_ ____(mol·L-1)-2;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(3)工业生产中用SO2为原料制取硫酸
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式___ ____________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式____ ______。
(4)工业生产中用氨水吸收SO2
若将等物质的量的SO2与NH3溶于水充分反应,写出该反应的离子方程式 ,所得溶液呈 性。
 、Cl-四种离子,某同学推测其离
、Cl-四种离子,某同学推测其离 子浓度大小顺序有如下四种关系:①c(Cl-)>c(NH
子浓度大小顺序有如下四种关系:①c(Cl-)>c(NH H
H 溶质,则该溶质是,上述四种离子浓度的大小顺序为(填序号)。
溶质,则该溶质是,上述四种离子浓度的大小顺序为(填序号)。 的pH=;
的pH=; 出的c(H+)=1.0×10-amol/L,设相同的pH的硫酸
出的c(H+)=1.0×10-amol/L,设相同的pH的硫酸 铝中水电离出的c(H+)=1.0×10-bmol/L(a、b都是小于14的正整数),那么a和b之间应满足的数量关系是(用一个等式和一个不等式表示)。、。
铝中水电离出的c(H+)=1.0×10-bmol/L(a、b都是小于14的正整数),那么a和b之间应满足的数量关系是(用一个等式和一个不等式表示)。、。 物质是由分子组成(填“极性分子”或“非极性分子”)
物质是由分子组成(填“极性分子”或“非极性分子”) 。
。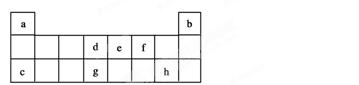
 质中熔点最高的可能是________(填字母)。
质中熔点最高的可能是________(填字母)。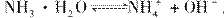 试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。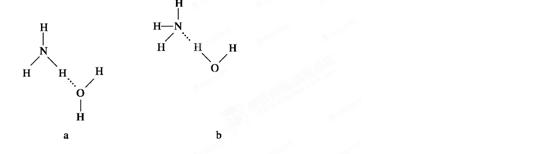
 上的主族元素性质相似,这称为对角线规则。据此请回答:
上的主族元素性质相似,这称为对角线规则。据此请回答: 粤公网安备 44130202000953号
粤公网安备 44130202000953号