酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)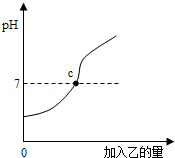
(1) ;
(2) ;
(3) .
酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)
(1) ;
(2) ;
(3) .