纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备方法是:
Ⅰ.将干燥后的金红石(主要成分是TiO2,主要杂质是SiO2)与碳粉混合放入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
Ⅱ.将SiCI4分离,得到纯净的TiCl4。
Ⅲ.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
Ⅳ.TiO2·xH2O高温分解得到TiO2。
①根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是 ,分离二者所采用的操作名称是 。
②Ⅲ中反应的化学方程式是 。
③如Ⅳ在实验室中完成,应将TiO2·xH2O放在 (填字母)中加热。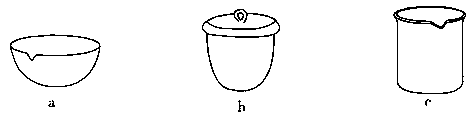
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2。H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
(3)某研究小组用下列装置模拟“生态马路”的部分原理。(夹持装置已略去)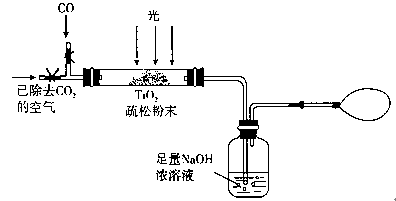
①如缓慢通入22.4 L(已折算成标准状况)CO气体,结果NaOH溶液增重11 g,则CO的转化率为 。
②当CO气体全部通入后,还要按图示通一段时间空气,其目的是 。
 、
、 、
、 、
、 和
和 分别填入下面对应的横线上,组成一个未配平的化学方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式。 。
。 的有_____________。
的有_____________。 ===
===
 ②
②

 ③
③

 ④
④

 ===
===
 ⑥
⑥



 粤公网安备 44130202000953号
粤公网安备 44130202000953号