以丙烯为原料合成高分子纤维P的路线如下: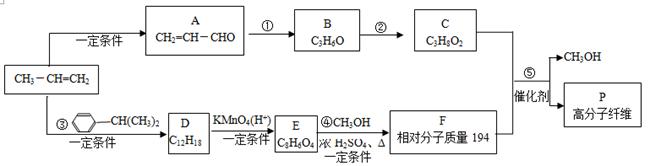
已知:RCOOR'+R"18OH RCO18OR"+R'OH
RCO18OR"+R'OH
(1)①的反应类型是______。
(2)C的核磁共振氢谱显示3个吸收峰,②的化学方程式是______。
(3)③是加成反应,D分子中苯环上的一氯代物只有一种。D的结构简式是______。
(4)④的化学方程式是______。
(5)P的结构简式是______。
以丙烯为原料合成高分子纤维P的路线如下:
已知:RCOOR'+R"18OH RCO18OR"+R'OH
RCO18OR"+R'OH
(1)①的反应类型是______。
(2)C的核磁共振氢谱显示3个吸收峰,②的化学方程式是______。
(3)③是加成反应,D分子中苯环上的一氯代物只有一种。D的结构简式是______。
(4)④的化学方程式是______。
(5)P的结构简式是______。