山梨酸是一种常用的食品防腐剂,以下是山梨酸的一种工业合成途径:
|

(2)
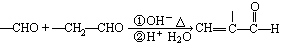
(3)
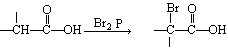
(4)

回答下列问题:
(1)E的结构简式为 ,含有官能团的名称 。
(2)G和H在一定条件下合成I的化学方程式为 ,反应类型为 。
(3)写出满足下列条件山梨酸的所有同分异构体
①分子中有五元碳环;②核磁共振氢谱有四个峰;③分子中有—COO—结构
(4)下列说法正确的是 。
A.I可以发生加成、取代、氧化、消去反应 B.I可以和新制的氢氧化铜反应
C.1molI完全燃烧可以消耗7molO2 D.J和等物质的量的H2加成有两种产物

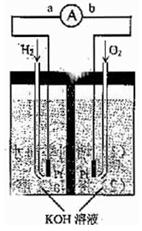
 2SO3(g)在一定条件下达到平衡,测得混合气体压强为原来的3/4,计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得混合气体压强为原来的3/4,计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。 2SO3,并达到平衡。则(填>、=、<;左、右;增大、减小、不变)。
2SO3,并达到平衡。则(填>、=、<;左、右;增大、减小、不变)。

 H2(g)
H2(g) 2NH3(g) △H < 0,其平衡常数K与温度T的关系如下表:
2NH3(g) △H < 0,其平衡常数K与温度T的关系如下表: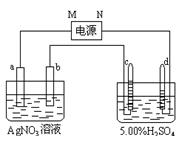
 ∶∶。
∶∶。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号