某地区使用含较少Ca2+、Mg2+的天然水按下列四个步骤制取自来水。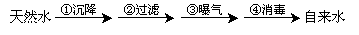
回答下列问题:
(1)该地区的天然水属于 (“硬水”或“软水”)
(2)在第一步中需要加入凝聚剂,常用的凝聚剂可以是 (任填一种凝聚剂名称)
(3)常用液氯作为消毒剂,其原理是
某地区使用含较少Ca2+、Mg2+的天然水按下列四个步骤制取自来水。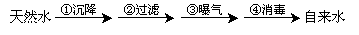
回答下列问题:
(1)该地区的天然水属于 (“硬水”或“软水”)
(2)在第一步中需要加入凝聚剂,常用的凝聚剂可以是 (任填一种凝聚剂名称)
(3)常用液氯作为消毒剂,其原理是