某工厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红(Fe2O3)和氧化铜。(已知铜能溶解在稀硝酸中生成硝酸铜溶液)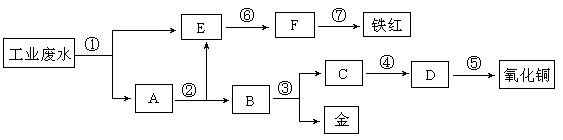
请填写下面空白:
(1)图中标号处需加入的相应物质分别是(填化学式)① ②
③ ④ ;
(2)A处固体成分为 (填化学式)
(3)写出⑤处反应的化学方程式 ;
某工厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红(Fe2O3)和氧化铜。(已知铜能溶解在稀硝酸中生成硝酸铜溶液)
请填写下面空白:
(1)图中标号处需加入的相应物质分别是(填化学式)① ②
③ ④ ;
(2)A处固体成分为 (填化学式)
(3)写出⑤处反应的化学方程式 ;