A、B、C、D、E、F是原子序数依次递增的前四周期元素。其中A与D同主族、C与E同主族,且E的原子序数是C的两倍;A分别与B和C均可形成10电子分子;B与C的最外层电子数之比2∶3;F原子的最外层电子数与A相同,其余各层均充满;常见化合物D2C2与水反应生成C的单质,其溶液可使酚酞试液变红。据此回答下列问题:
(1)F元素形成的高价基态离子的核外电子排布式为 ;C、D、E三元素原子均能形成简单离子,其离子半径大小顺序为 (用离子符号表示);
(2)A与C形成的10电子分子中含的化学键类型为 (填σ键或π键),分子中心原子的轨道杂化类型为 ,其化合物晶体类型为 ;化合物A2C和A2E中,沸点较高的是 (填分子式);
(3)向含1 mol A2E的水溶液中加入等物质的量的D2C2,有黄色沉淀生成,写出离子方程式 :
(4)常温常压下,有23 g液态化合物B2A6C与足量的C的单质充分反应,生成BC2气体和A2C液体,同时放出683.5 kJ的热量,该反应的热化学方程式为: 。
 2NH3(g)
2NH3(g)
 号)
号)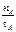 mol·L-1·min-1
mol·L-1·min-1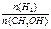 增大
增大 粤公网安备 44130202000953号
粤公网安备 44130202000953号