甲、乙、丙三种同体物质的溶解度曲线如图所示,请回答下列问题:
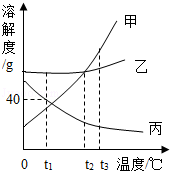
(1)
℃时,三种物质中溶解度最大的是.
(2)使
℃时接近饱和的甲溶液变为饱和溶液,可采用的一种方法是.
(3)
℃时,将50
水放入盛有30
丙物质的烧杯中,充分搅拌,所得溶液的质量为
.
(4)将
℃时甲、乙两种物质的饱和溶液降温到
℃,析出晶体的质量关系为(填字母).
| A. | 甲>乙 | B. | 甲<乙 | C. | 甲=乙 | D. | 无法确定 |
甲、乙、丙三种同体物质的溶解度曲线如图所示,请回答下列问题:

(1)
℃时,三种物质中溶解度最大的是.
(2)使
℃时接近饱和的甲溶液变为饱和溶液,可采用的一种方法是.
(3)
℃时,将50
水放入盛有30
丙物质的烧杯中,充分搅拌,所得溶液的质量为
.
(4)将
℃时甲、乙两种物质的饱和溶液降温到
℃,析出晶体的质量关系为(填字母).
| A. | 甲>乙 | B. | 甲<乙 | C. | 甲=乙 | D. | 无法确定 |