已知A、B、C、D、E是 初中化学中常见的五种物质.其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D中含有金属元素,该金属元素的单质是世界年产量最高的金属.它们在一定条件下的转化关系如图所示(→表示转化).请回答下列问题:
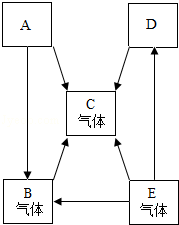
(1)A物质是;
(2)评价物质B的"利"与"弊"(各写一例)利:; 弊:.
(3)写出E转化为D的化学方程式:.
已知A、B、C、D、E是 初中化学中常见的五种物质.其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D中含有金属元素,该金属元素的单质是世界年产量最高的金属.它们在一定条件下的转化关系如图所示(→表示转化).请回答下列问题:

(1)A物质是;
(2)评价物质B的"利"与"弊"(各写一例)利:; 弊:.
(3)写出E转化为D的化学方程式:.