现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动:
可选用试剂:浓H2SO4、浓HNO3、10%盐酸、0.1mol/LH2SO4、0.1mol/LHNO3、0.1mol/LBaCl2、0.1mol/LBa(NO3)2、3%H2O2、10%NaOH溶液、蒸馏水、品红溶液;仪器自选。
(1)提出假设
假设一:固体全部是Na2SO3; 假设二:固体全部是Na2SO4;
假设三: 。
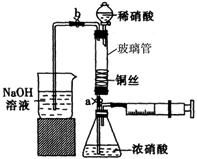
(2)设计实验方案(略);选用下图装置进行实验,该装置的优点是 。
(3)进行实验:请在下表中用简要文字写出实验操作、预期现象和结论。
| 实验步骤 |
预期现象和结论 |
| 步骤1:取适量固体样品于微型试管中;在W管a处滴入 、b处滴入 ;用胶管将W管与微型试管连接好 |
|
| 步骤2:用针筒吸入 ,将针头穿过微型试管的胶塞,向固体样品中注入该溶液。 |
。 |
| 步骤3:拨出针筒,吸入蒸馏水洗净;再吸入 注入微型试管中 |
。 |
(4)若将上述探究过程中生成的气体通入到足量的新制漂白粉浓溶液中,则可生成白色沉淀。试写出该反应的离子方程式: 。





 粤公网安备 44130202000953号
粤公网安备 44130202000953号