S2C12是一种金黄色易挥发的液体,常用作橡胶硫化剂。某化学兴趣小组拟设计实验制备少量的S2C12,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化合价升高,另一部分化合价降低)。加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2C12,反应的化学方程式为:2S+Cl2 S2Cl2。
S2Cl2。
反应涉及的几种物质的熔沸点如下:
| 物质 |
S |
S2Cl2 |
| 沸点/℃ |
445 |
138 |
| 熔点/℃ |
113 |
-76 |
该小组设计的制备装置如下图(夹持仪器已略去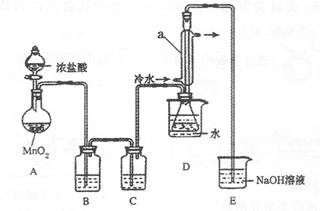
回答下列问题:
(1)连接好实验装置后的第一步实验操作是______。
(2)实验中需要加热的仪器是______。(填写字母)
(3)装置B、C中的试剂分别是______。
(4)装置D中仪器a的作用是______。
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是____________。
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因____________
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气体产生。用离子方程式表示产生该现象的原因____________。
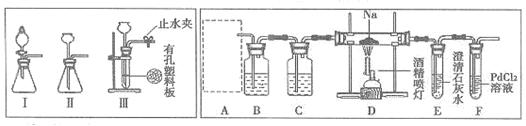 已知:常温下,CO能使一些化合物中的金属离子被还原。
已知:常温下,CO能使一些化合物中的金属离子被还原。

 因是
因是 __________乙同学:根据甲同学改进后计算硫酸铵化肥的氮含量又可能偏低,因为实验装置中还存在另一个明显缺陷是:____________________________
__________乙同学:根据甲同学改进后计算硫酸铵化肥的氮含量又可能偏低,因为实验装置中还存在另一个明显缺陷是:____________________________ 后的实验装置重新进行实验,测得实验前后B装置增重3.40g。该化肥_________
后的实验装置重新进行实验,测得实验前后B装置增重3.40g。该化肥_________ (填“是”或“不是”)一等品。
(填“是”或“不是”)一等品。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号