“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: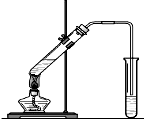
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
| A.加成反应 | B.取代反应 | C.水解反应 | D.酯化反应 |
⑶反应中浓硫酸的作用是:
⑷写出制取乙酸乙酯的化学反应方程式:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
| A.加成反应 | B.取代反应 | C.水解反应 | D.酯化反应 |
⑶反应中浓硫酸的作用是:
⑷写出制取乙酸乙酯的化学反应方程式: