某有机物A含C:54.8%,H:5.58%,N:7.11%,其余含O,A的相对分子质量不超过300。A是氨基酸,分子中不存在甲基(-CH3),能与FeCl3溶液发生显色反应,1molA最多能与3molNaOH完全反应。请回答:
(1)有机物A的相对分子质量为 ,其分子式为 。
(2)符合上述条件的有机物A的可能结构有 (填数字)种,其中核磁共振氢谱为7组峰,且峰面积为1:2:2:2:2:1:1的α-氨基酸中的任一种的结构简式 。
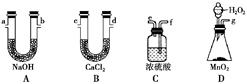
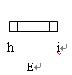
 知:①当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位。
知:①当苯环上连有甲基时,再引入的其他基团主要进入甲基的邻位或对位;当苯环上连有羧基时,再引入的其他基团主要进入羧基的间位。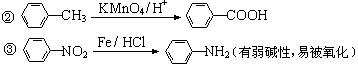
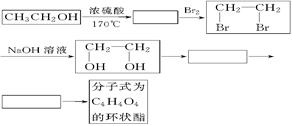
 中含有的含氧官能团的名称为 。
中含有的含氧官能团的名称为 。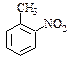 、
、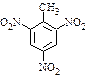 等
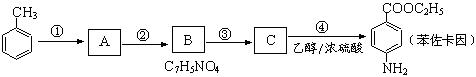
等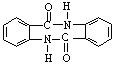 有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图。
有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图。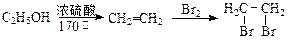
 粤公网安备 44130202000953号
粤公网安备 44130202000953号