有下列各组微粒或物质:
A.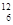 C和 C和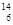 C C |
B.CH3CH2CH2CH3和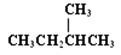 |
C.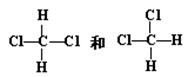 |
D.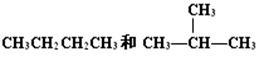 |
(1)__________组两种微粒互为同位素;
(2)__________组两种物质属于同系物;
(3)__________组两种物质互为同分异构体;
(4)__________组两种物质是同一物质。
有下列各组微粒或物质:
A.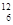 C和 C和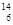 C C |
B.CH3CH2CH2CH3和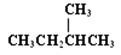 |
C.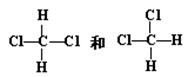 |
D.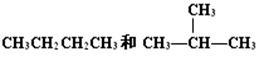 |
(1)__________组两种微粒互为同位素;
(2)__________组两种物质属于同系物;
(3)__________组两种物质互为同分异构体;
(4)__________组两种物质是同一物质。