右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。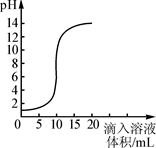
(1)根据曲线判断,该反应是将 (填“氢
氧化钠溶液”或“盐酸”,下同)滴入 中,
理由是 。
(2)当滴入溶液的体积为15mL时,所得溶液中的溶质为 (写化学式)。
右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)根据曲线判断,该反应是将 (填“氢
氧化钠溶液”或“盐酸”,下同)滴入 中,
理由是 。
(2)当滴入溶液的体积为15mL时,所得溶液中的溶质为 (写化学式)。