在密闭容器中,保持一定温度进行如下反应N2(g)+ 3H2(g) 2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成a mol NH3,在恒容条件下达到平衡时生成b mol NH3(见下表中编号①的一行)。若相同条件下,达到平衡时混合物中各组分的百分含量不变。回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。
(2)平衡常数K值越大,表明建立平衡时 (填字母序号)。
| A.N2的转化率越高 | B.NH3的产量越大 |
| C.正反应进行得越彻底 | D.化学反应速度越快 |
(3)a与b的关系是:a b(填>、<、=)
(4)填写下表空格:
| 状态 条件 |
起始时物质的物质的量(mol) |
平衡时NH3的物质的量 (mol) |
|||
| 编号 |
X(N2) |
Y(H2) |
Z(NH3) |
||
| 恒容 |
① |
1 |
3 |
0 |
b |
| ② |
0 |
0 |
|
b |
|
| ③ |
|
2.25 |
|
b |
 p C在某温度下达到平衡
p C在某温度下达到平衡 cC(气)+dD(气);ΔH=Q,根据图回答:
cC(气)+dD(气);ΔH=Q,根据图回答:
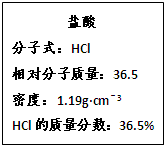
 MnCl2+Cl2↑+2H2O,其中
MnCl2+Cl2↑+2H2O,其中 粤公网安备 44130202000953号
粤公网安备 44130202000953号